周期表とその見方 戻る
性質のよく似た元素が縦の列に並ぶように整理した表を周期表といいいます。
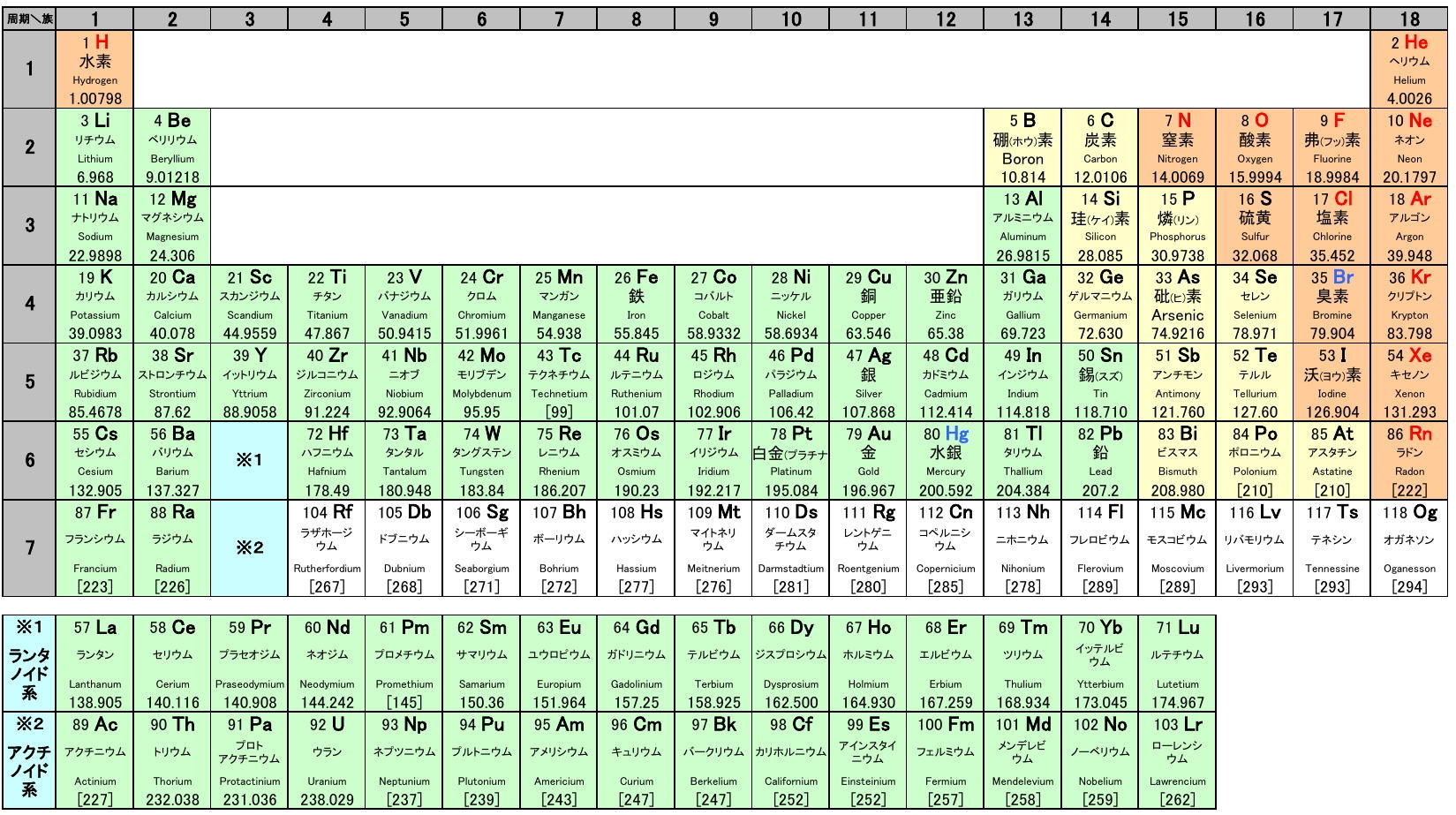

元素の整理
族と周期、同族元素
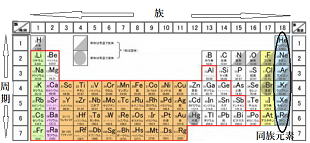
電子の配置と価電子
| 価電子とは |
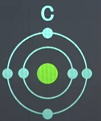 |
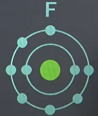 |
| 最外殻電子の数 |
4 |
7 |
| 価電子の数 |
4 |
7 |
| 価電子: 最外殻にある1から7個の電子 |
内側からn番目の電子殻が含む電子の最大収容数は、2n2個
希ガスの電子配置
希ガス:He(ヘリウム) Ne(ネオン) Ar(アルゴン) Kr(クリプトン) Xe(キセノン) Rn(ラドン)
 |
| 元素 |
電子殻 |
| K L M N |
| He |
2 |
| Ne |
2 8 |
| Ar |
2 8 8 |
| Kr |
2 8 18 8 |
(ルール)
希ガスの価電子は0個である |
 |
問 下図は窒素とネオンの原子を模式的に示しています。
次の各問いに答えなさい。
 
(1) 窒素原子は最外殻に5つの電子をもっています。それらの電子をなんといいますか?
(2) ネオン原子の価電子はいくつありますか?
(3) ネオンのL殻のように、最大数の原子が収容された電子殻をなんといいますか
(4) He、 Ne、 Ar、 Kr(クリプトン) Xe(キセノン) Rnの6種の元素を何といいますか? |
解答
(1) (1から7までを)価電子 (2) (希ガスなので) 0
(3) 閉殻 (4) 希ガス
周期律と価電子
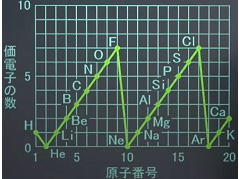
周期律:元素を原子番号の順に並べたとき、その性質が周期的に変化するルールのこと
元素の分類
1.典型元素
周期表の1族、2族、12~18族の元素を典型元素という。典型元素には、単体が金属の性質を示す金属元素と、それ以外の非金属元素がある。
典型元素では、原子番号の増加に伴って、価電子の数が周期的に変化する。そのため同じ族の価電子の数が等しく、周期表中の上下の元素の間で性質がよく似ている。
特に性質が似ている族の元素には、特別な名称がつけられている。
- アルカリ金属:水素以外の1族の元素
- アルカリ土類金属:Be、Mgを除く2族の元素
- ハロゲン:17族の元素
- 希ガス:18族の元素
2.遷移元素
3~11族の元素を遷移元素という。遷移元素では、原子番号が増加しても、価電子の数は1または2であるものが多い。このため、となり同士の元素の間で比較的似た性質を示す。遷移元素はすべて金属元素である。
金属元素と非金属元素
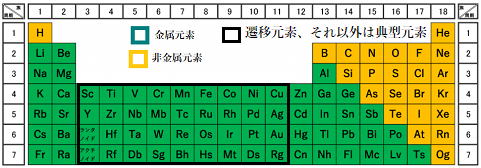 緑色の領域に該当する元素が金属元素、オレンジ色が非金属元素です。
緑色の領域に該当する元素が金属元素、オレンジ色が非金属元素です。
金属元素 …光沢、電気伝導性、熱伝導性 但し、Geなどは半金属です
元素のうち、単体が金属光沢を持ち、電気や熱をよく導くものを金属元素という(元素の8割を占めている)。
金属元素は陽性が強く、化合物をつくるときに陽イオンになりやすい。
※周期表の左側かつ下側にある金属元素ほど陽性が強い。もっとも陽性が強いのは、フランシウムFrである。
非金属元素
金属元素以外の元素を非金属元素という(すべて典型元素である)。
非金属元素は陰性が強いものが多く、陰イオンになりやすい(希ガスを除く)。
※下図のように周期表の右側かつ上側にある非金属元素ほど陰性が強い。もっとも陰性が強いのは、フッ素Fである(但し、希ガスを除く)
陽性と陰性
陽性:価電子を失って、陽イオンになりやすい性質 水素や金属元素 左下
陰性:電子を取り込んで、陰イオンになりやすい性質 塩素や酸素また硫黄などの非金属元素は陰性元素 右上(希ガスを除く)
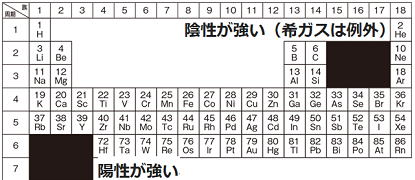
・遷移元素(3~11)と典型元素
・アルカリ金属(1族の水素を除く)とアルカリ土類金属(2族のBeとMgを除く)
ハロゲン、希ガス
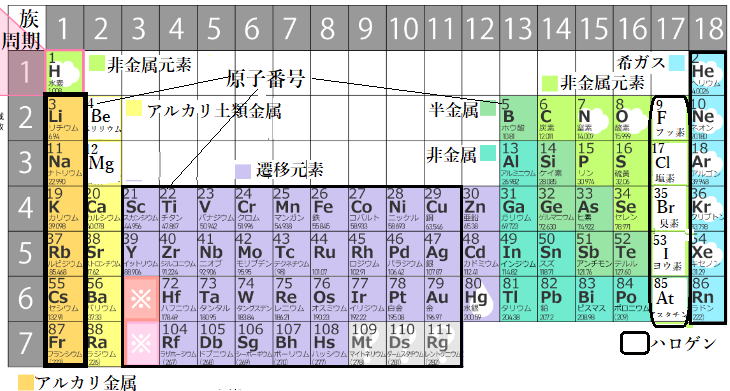
縦の列を族、横の行を周期といい、同族であれば価電子数が同じなので化学的性質が似ています。
例えばLi,Na,Kは同じ族に入ります。同周期であれば※最外殻の種類が同じです。
また、元素を原子番号の順に並べると元素の化学的性質が一定の周期で変わっていくことを周期律といいます。
典型元素と遷移元素の領域とその性質も覚えておきましょう。
・典型元素の性質
化学的性質(反応性) … 縦(同族)で似ている
化合物の色 … 無色が多い
・遷移元素の性質
化学的性質(反応性) … 横(同周期)で似ている
化合物の色 … 有色が多い
気体
水素H2、窒素N2、酸素O2、フッ素F2、塩素Cl2、希ガス(6個すべて) で合計11個
液体
臭素Br2、水銀Hg で合計2個
固体
その他全部
※最外殻の種類が同じ元素を横列にする。後で学習します。
第1周期(K殻),第2周期(L殻),…
※【族】主に最外殻の電子数の同じ元素を縦列にする。
同族元素:価電子数が同じであるために化学的性質が似ています。
原子番号1~20番の語呂合わせ
原子番号1~20番は必ず覚えましょう。一般的に以下の語呂合わせが用いられています。
| H |
He |
Li |
Be |
B |
C |
N |
O |
F |
Ne |
Na |
Mg |
Al |
Si |
P |
S |
Cl |
Ar |
K |
Ca |
| 水 |
兵 |
リー |
べ |
|
ク |
の |
船 |
な |
まが |
あーる |
シッ |
プ |
ス |
クラーク |
か |
問1 (1) 上の原子番号1~20番の原子名を答えなさい。
(2) 元素を原子番号の順に並べたとき、その性質が周期的に変化するルールのことをなんというか
(3) (2)に基づき性質の似た元素が縦に並ぶように配列した表をなんというか
(4) 周期表の横の列、縦の列をそれぞれなんというか
(5) 同じ縦の列に属する元素のことをなんというか
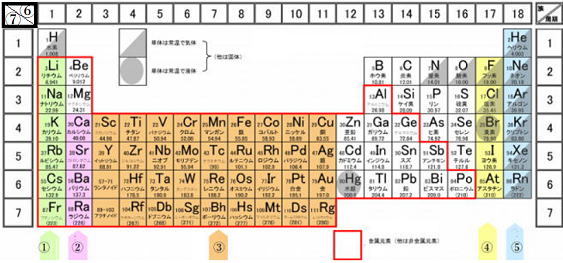
問2 ①から⑦までをなんと呼びますか?名称を答えなさい。
① ( ) ② ( ) ③ ( ) ④ ( )
⑤ ( ) ⑥ ( ) ⑦ ( )
|
問1答
(1)水素 ヘリウム リチウム ベリリウム ホウ素 炭素 窒素 酸素 フッ素 ネオン
ナトリウム マグネシウム アルミニウム ケイ素 リン 硫黄 塩素 アルゴン
カリウム カルシウム (2)周期律 (3)周期表 横:周期 縦:族 (4)同族元素
問3 正しいものには〇、誤っているものには×をつけなさい。×は、またその理由を述べよ。
(1) 希ガスとは18族元素のことを指す。
(2) 希ガスの電子配置は安定しており、化学反応をほとんどおこさない。
(3) 希ガスの最外殻電子の数は、すべて8である。
(4) 希ガスの価電子の数はすべて0である。
(5) 1族元素はすべてアルカリ金属である。
(6) 2族元素はすべてアルカリ土類金属である。
(7) 17族元素は非金属元素である。
(8) 18族元素は陰性が大きい。 |
問3解答
(1) 希ガスとは18族元素のことを指す。〇
(2) 希ガスの電子配置は安定しており、化学反応をほとんどおこさない。〇
第18族元素は、原子における最外殻電子が閉殻なっているため、化学的に非常に不活性であり、しばしば単原子分子として存在する。かつて第18族元素には化合物が知られていなかったために、化学反応を起こさないという意味で不活性ガス(inert
gas)類と呼ばれた。しかし、化学的な不活性さの度合いは、第1周期元素のヘリウムを筆頭として、周期が進むにつれて弱くなる。安定核種が存在する最後の周期である第5周期のキセノンに化合物が見つかったことを皮切りに、現在では他の第18族元素にも化合物が見つかっており、完全に不活性というわけではない。(Wikipedia)
(3) 希ガスの最外殻電子の数は、すべて8である。× Heだけ2個
(4) 希ガスの価電子の数はすべて0である。〇
(5) 1族元素はすべてアルカリ金属である。 × 水素は除く
(6) 2族元素はすべてアルカリ土類金属である。× BeとMgはアルカリ土類金属でない
(7) 17族元素は非金属元素である。〇
(8) 18族元素は陰性が大きい。 × 希ガスは安定している
ちなみに、陰性が大きのは17族元素のハロゲン













